Trans efekt - Trans effect
v anorganická chemie, trans efekt je labilizace (reaktivnější) z ligandy to jsou trans na určité další ligandy, které lze tedy považovat za trans-směrující ligandy. Je to přičítáno elektronické efekty a je nejpozoruhodnější ve čtvercovém planárním tvaru komplexy, ačkoli to lze pozorovat také pro oktaedrické komplexy.[1] The cis efekt je nejčastěji pozorován v oktaedrických komplexech přechodových kovů.
Kromě toho kinetický trans efekt, trans ligandy mají také vliv na základní stav molekuly, z nichž nejpozoruhodnější jsou délky vazby a stabilita. Někteří autoři dávají přednost tomuto pojmu trans vliv odlišit jej od kinetického efektu,[2] zatímco jiní používají konkrétnější termíny jako např strukturální trans efekt nebo termodynamický trans efekt.[1]
Objev trans efektu je přičítán Ilya Ilich Černyajev,[3] kdo jej poznal a dal mu jméno v roce 1926.[4]
Kinetický trans efekt
Intenzita trans efektu (měřená zvýšením rychlosti substituce trans ligandu) sleduje tuto sekvenci:
- F−, H2Ó, ACH− < NH3 < py < Cl− < Br− < Já−, SCN−, NE2−, SC (NH2)2, Ph− < TAK32− < PR3, AsR3, SR2, CH3− < H−, NE, CO, CN−, C2H4
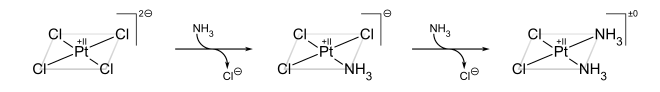
Klasickým příkladem trans efektu je syntéza cisplatina a jeho trans izomer.[5] Počínaje PtCl42−, první NH3 ligand je přidán do libovolné ze čtyř ekvivalentních pozic náhodně. Protože však Cl− má větší trans účinek než NH3, druhý NH3 je přidán trans do Cl− a proto cis k prvnímu NH3.
Pokud naopak začíná jeden z Pt (NH3)42+, trans místo toho se získá produkt:
Trans efekt ve čtvercových komplexech lze vysvětlit pomocí mechanismu přidání / eliminace, který prochází trigonálním bipyramidovým meziproduktem. Ligandy s vysokým trans efektem jsou obecně ty s vysokou kyselostí π (jako v případě fosfinů) nebo s nízkým ligandem - volný pár – dπ repulze (jako v případě hydridu), které upřednostňují více π-bazických rovníkových míst v meziproduktu. Druhá rovníková poloha je obsazena příchozím ligandem; v důsledku princip mikroskopické reverzibility musí odcházející ligand také opustit z rovníkové polohy. Třetí a poslední rovníkové místo je obsazeno trans ligandem, takže čistým výsledkem je, že kineticky zvýhodněný produkt je ten, ve kterém je ligand trans vyloučen s největším trans efektem.[2]
Strukturální trans efekt
Strukturní trans efekt lze měřit experimentálně pomocí Rentgenová krystalografie a je pozorováno jako protahování vazeb mezi kovem a ligandem trans na trans-ovlivňující ligand. U silných trans ovlivňujících ligandů, jako je hydrid, dochází k protahování až o 0,2 Á. A cis vliv lze také pozorovat, ale je menší než trans vliv. Relativní důležitost vlivů cis a trans závisí na formální elektronové konfiguraci centra kovu a byla navržena vysvětlení založená na zapojení atomových orbitalů.[6]
Reference
- ^ A b Coe, B. J .; Glenwright, S. J. Trans-efekty v oktaedrických komplexech přechodových kovů. Recenze koordinační chemie 2000, 203, 5-80.
- ^ A b Robert H. Crabtree (2005). Organokovová chemie přechodných kovů (4. vydání). New Jersey: Wiley-Interscience. ISBN 0-471-66256-9.
- ^ Kauffmann, G. B. I'lya I'lich Chernyaev (1893-1966) a Trans Effect. J. Chem. Educ. 1977, 54, 86-89.
- ^ Černyajev, I. I. Mononitrity bivalentní platiny. I. Ann. inst. platina (SSSR) 1926, 4, 243-275.
- ^ George B.Kauffman, Dwaine O. Cowan (1963). "cis- a trans-Dichlorodiammineplatinum (II) ". Inorg. Synth. 7: 239–245. doi:10.1002 / 9780470132388.ch63.CS1 maint: používá parametr autoři (odkaz)
- ^ Anderson, K. M .; Orpen, A. G. O relativních velikostech cis a trans vlivy v kovových komplexech. Chem. Commun. 2001, 2682-2683. doi:10.1039 / b108517b
Další čtení
- Quagliano, J. V .; Schubert, Leo. Trans účinek v komplexních anorganických sloučeninách. Chem. Rev. 1952, 50, 201-260. doi:10.1021 / cr60156a001
- Basolo, F.; Pearson, R. G. Trans efekt v kovových komplexech. Prog. Inorg. Chem. 1962, 4, 381-453.
- Hartley, F. R. Cis- a trans-účinky ligandů. Chem. Soc. Rev. 1973, 2, 163-179. doi:10.1039 / CS9730200163